I riassunti , gli appunti i testi contenuti nel nostro sito sono messi a disposizione gratuitamente con finalità illustrative didattiche, scientifiche, a carattere sociale, civile e culturale a tutti i possibili interessati secondo il concetto del fair use e con l' obiettivo del rispetto della direttiva europea 2001/29/CE e dell' art. 70 della legge 633/1941 sul diritto d'autore
Le informazioni di medicina e salute contenute nel sito sono di natura generale ed a scopo puramente divulgativo e per questo motivo non possono sostituire in alcun caso il consiglio di un medico (ovvero un soggetto abilitato legalmente alla professione).
LA CONCENTRAZIONE DELLE SOLUZIONI
I modi di esprimere la concentrazione delle soluzioni che prenderemo in considerazione sono i seguenti:
I) Grammi/litro: grammi di soluto contenuti in un litro di soluzione.
II) Molarità (M): moli di soluto contenuti in un litro di soluzione.
III) % p/p: grammi di soluto contenuti in 100 grammi di soluzione.
IV)% p/v: grammi di soluto contenuti in 100 ml di soluzione.
V) Normalità: equivalenti di soluto contenuti in un litro di soluzione.
Occorre tenere presente che esistono molti altri modi di esprimere la concentrazione, che normalmente non vengono utilizzati nel laboratorio di analisi:
VI) % v/v: ml di soluto contenuti in 100 ml di soluzione. Viene usata per le soluzioni liquido-liquido (Es. acqua-alcol)
VII) Molalità (m): moli di soluto contenute in un chilogrammo di solvente puro. Viene utilizzata in chimica-fisica
VIII) Parti per milione (ppm): grammi di soluto contenute in un milione di grammi (1000 Kg) di soluzione. Equivalgono a mg/litro e sono usati per definire la concentrazione di specie presenti in quantità minime.
IX) Frazione molare (X): numero di moli della specie considerata diviso il numero di moli totali.
Per risolvere i problemi relativi alle soluzioni occorre saper esprimere le moli nel modo più opportuno, secondo il sistema che stiamo trattando:
A) Solido. Il numero di moli contenute in una determinata quantità di grammi di sostanza solida pura si ricava dalla relazione:
|
B) Soluzione di cui è nota la molarità M: Per ricavare il numero di moli contenute in un volume V (espresso in ml) di soluzione avente molarità M si usa la seguente relazione:
|
C) Soluzione di cui è nota la percentuale p/p e la densità d (g/ml): Vogliamo ricavare il numero di moli di soluto contenute in V ml di soluzione di cui conosciamo la % p/p e la densità d. Sappiamo che:
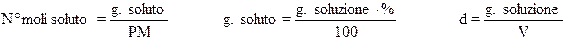
Combinando le tre espressioni si ricava:
|
D) Soluzione di cui è nota la percentuale p/v:
Conosciamo la % p/v di una soluzione e vogliamo sapere quante moli di soluto sono contenute in V ml di soluzione. Sapendo che:

Si ricava che:
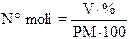 |
Concentrazione di una soluzione
Fonte: http://www.chimicaescuola.altervista.org/alterpages/files/LACONCENTRAZIONEDELLESOLUZIONI.doc
Sito web da visitare: http://www.chimicaescuola.altervista.org/
Autore del testo: non indicato nel documento di origine
Il testo è di proprietà dei rispettivi autori che ringraziamo per l'opportunità che ci danno di far conoscere gratuitamente i loro testi per finalità illustrative e didattiche. Se siete gli autori del testo e siete interessati a richiedere la rimozione del testo o l'inserimento di altre informazioni inviateci un e-mail dopo le opportune verifiche soddisferemo la vostra richiesta nel più breve tempo possibile.
I riassunti , gli appunti i testi contenuti nel nostro sito sono messi a disposizione gratuitamente con finalità illustrative didattiche, scientifiche, a carattere sociale, civile e culturale a tutti i possibili interessati secondo il concetto del fair use e con l' obiettivo del rispetto della direttiva europea 2001/29/CE e dell' art. 70 della legge 633/1941 sul diritto d'autore
Le informazioni di medicina e salute contenute nel sito sono di natura generale ed a scopo puramente divulgativo e per questo motivo non possono sostituire in alcun caso il consiglio di un medico (ovvero un soggetto abilitato legalmente alla professione).
"Ciò che sappiamo è una goccia, ciò che ignoriamo un oceano!" Isaac Newton. Essendo impossibile tenere a mente l'enorme quantità di informazioni, l'importante è sapere dove ritrovare l'informazione quando questa serve. U. Eco
www.riassuntini.com dove ritrovare l'informazione quando questa serve