I riassunti , gli appunti i testi contenuti nel nostro sito sono messi a disposizione gratuitamente con finalità illustrative didattiche, scientifiche, a carattere sociale, civile e culturale a tutti i possibili interessati secondo il concetto del fair use e con l' obiettivo del rispetto della direttiva europea 2001/29/CE e dell' art. 70 della legge 633/1941 sul diritto d'autore
Le informazioni di medicina e salute contenute nel sito sono di natura generale ed a scopo puramente divulgativo e per questo motivo non possono sostituire in alcun caso il consiglio di un medico (ovvero un soggetto abilitato legalmente alla professione).
La cristallizzazione è una operazione unitaria i cui obiettivo è quello di ottenere un solido allo stato cristallino a partire da una soluzione più o meno concentrata. Il principio su cui si basa la cristallizzazione è quello di provocare la sovrassaturazione delle soluzioni e la conseguente precipitazione dei cristalli di soluto.
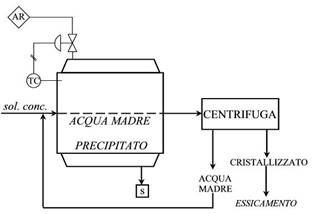 La soluzione che entra nel cristallizzatore proveniente dal concentratore, deve avere una concentrazione tale da far precipitare il soluto per semplice raffreddamento. La soluzione all’interno del cristallizzatore, si miscela con l’acqua di raffreddamento che abbassa la sua temperatura e di conseguenza, il soluto precipita. Ora la soluzione è divisa in due fasi: l’acqua madre e il soluto. Tutto questo viene mandato ad una centrifuga che separa l’acqua madre e il cristallizzato. L’acqua madre viene riciclata in testa al cristallizzatore per due motivi: perché contiene ancora soluto e anche perché contiene microcristalli per l’inseminazione. Il cristallizzato viene sottoposto ad essiccamento per eliminare l’umidità ancora presente.
La soluzione che entra nel cristallizzatore proveniente dal concentratore, deve avere una concentrazione tale da far precipitare il soluto per semplice raffreddamento. La soluzione all’interno del cristallizzatore, si miscela con l’acqua di raffreddamento che abbassa la sua temperatura e di conseguenza, il soluto precipita. Ora la soluzione è divisa in due fasi: l’acqua madre e il soluto. Tutto questo viene mandato ad una centrifuga che separa l’acqua madre e il cristallizzato. L’acqua madre viene riciclata in testa al cristallizzatore per due motivi: perché contiene ancora soluto e anche perché contiene microcristalli per l’inseminazione. Il cristallizzato viene sottoposto ad essiccamento per eliminare l’umidità ancora presente.
Rappresentando le reazioni di solubilizzazione, possiamo scrivere: solido + n · H2O → soluzione ± calore. Questo tipo di reazioni possono essere esotermiche o endotermiche, nella maggior parte dei casi le reazioni di dissoluzione sono endotermiche (richiedono calore). La solubilità, quindi, dipende dalla temperatura. Nella maggior parte dei casi la solubilità cresce al crescere della temperatura. Le curve della solubilità sono il luogo dei punti che rappresentano le concentrazioni di saturazione al variare della temperatura. Una soluzione si dice satura quando si è in presenza del precipitato.
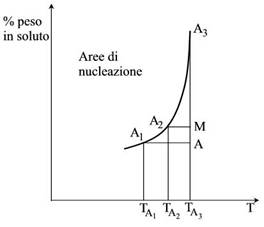 Tecniche di cristallizzazione
Tecniche di cristallizzazioneConsiderando una qualunque curva di solubilità, i punti a destra della curva (es.: A), sono relativi a soluzione insature, in cui è possibile sciogliere ancora il soluto.
Partendo da una soluzione insatura (A), la cristallizzazione può essere ottenuta nei seguenti modi:
Il processo di cristallizzazione è il risultato di due fasi consecutive: la formazione dei germi cristallini (nucleazione) e la fase di accrescimento dei cristalli.
Le due fasi sono caratterizzate rispettivamente da una velocità di nucleazione e da una velocità di accrescimento. Il rapporto tra queste due velocità è in relazione con le dimensioni dei cristalli ottenuti. Se si verifica che Vnucl > Vaccr, allora otterremo un elevato numero di cristalli, ma di dimensioni relativamente piccole. Nel caso che Vaccr > Vnucl, avremo relativamente pochi cristalli di grandi dimensioni. Nel caso in cui le due velocità siano comparabili, il precipitato sarà ovviamente di medie dimensioni.
Il fenomeno della nucleazione è influenzato direttamente dalla sovrassaturazione della soluzione. Infatti, tanto è maggiore la sovrassaturazione della soluzione tanto è più facilmente si aggregano le molecole del soluto per formare centri di aggregazione.
Il grado di sovrassaturazione influenza anche le dimensioni dei cristalli. Nel caso di elevate sovrassaturazione, si formeranno molti centri di aggregazione, e di conseguenza i cristalli raggiungeranno dimensioni ridotte; invece se abbiamo una sovrassaturazione modesta si formeranno pochi centri di nucleazione che formeranno cristalli di elevate dimensioni.
Altri accorgimenti atti a fornire cristalli di grandi dimensioni possono essere utilizzati in casi particolari:
La presenza di impurezze può in centri casi modificare la forma dei cristalli ottenuti (modificazioni reticolari).
Il rendimento dell’operazione di cristallizzazione si calcola effettuando un bilancio di materia. I cristalli che si formano possono essere anidri o idratati. Il bilancio sarebbe: soluzione conc. = acqua madre + cristallizzato, in formula matematica: Ms = C + Mr.
Ms = soluto in ingresso
C = cristallizzato
Mr = soluto nell’acqua madre
Per il calcolo della massa residua si ha:
![]()
S = solubilità = g soluto / 100 g solvente
Da cui si può calcolare C:
![]()
se non si è verificata evaporazione di solvente la Msolv sarà identica a quella iniziale, in caso contrario Msolv dovrà essere sostituita con Mf, massa all’uscita del cristallizzatore (finale).
Alcuni sali inglobano molecole di H2O (si idratano) nelle molecole di cristallizzazione, quindi si ha una massa maggiore di quella iniziale. C diventerà:
![]()
Ci = crist. Idrato
Pan = PM del sale anidro
Pi = PM del sale idrato
La resa di cristallizzazione è il rapporto tra la massa si soluto cristallizzato e la massa di soluto iniziale:
![]()
Le apparecchiature usate per la cristallizzazione possono essere classificate in base alle tecniche di cristallizzazione impiegate in:
Fonte: http://members.xoom.virgilio.it/alberto_chim/la%20cristallizzazione.doc
Sito web da visitare: http://members.xoom.virgilio.it/alberto_chim
Autore del testo: non indicato nel documento di origine
Il testo è di proprietà dei rispettivi autori che ringraziamo per l'opportunità che ci danno di far conoscere gratuitamente i loro testi per finalità illustrative e didattiche. Se siete gli autori del testo e siete interessati a richiedere la rimozione del testo o l'inserimento di altre informazioni inviateci un e-mail dopo le opportune verifiche soddisferemo la vostra richiesta nel più breve tempo possibile.
I riassunti , gli appunti i testi contenuti nel nostro sito sono messi a disposizione gratuitamente con finalità illustrative didattiche, scientifiche, a carattere sociale, civile e culturale a tutti i possibili interessati secondo il concetto del fair use e con l' obiettivo del rispetto della direttiva europea 2001/29/CE e dell' art. 70 della legge 633/1941 sul diritto d'autore
Le informazioni di medicina e salute contenute nel sito sono di natura generale ed a scopo puramente divulgativo e per questo motivo non possono sostituire in alcun caso il consiglio di un medico (ovvero un soggetto abilitato legalmente alla professione).
"Ciò che sappiamo è una goccia, ciò che ignoriamo un oceano!" Isaac Newton. Essendo impossibile tenere a mente l'enorme quantità di informazioni, l'importante è sapere dove ritrovare l'informazione quando questa serve. U. Eco
www.riassuntini.com dove ritrovare l'informazione quando questa serve