I riassunti , gli appunti i testi contenuti nel nostro sito sono messi a disposizione gratuitamente con finalità illustrative didattiche, scientifiche, a carattere sociale, civile e culturale a tutti i possibili interessati secondo il concetto del fair use e con l' obiettivo del rispetto della direttiva europea 2001/29/CE e dell' art. 70 della legge 633/1941 sul diritto d'autore
Le informazioni di medicina e salute contenute nel sito sono di natura generale ed a scopo puramente divulgativo e per questo motivo non possono sostituire in alcun caso il consiglio di un medico (ovvero un soggetto abilitato legalmente alla professione).
LA FISICA QUANTISTICA
Dalla seconda metà del XIX secolo la fisica poteva dirsi assestata: la maggior parte dei fenomeni trovava spiegazione
Alcuni fenomeni erano, tuttavia irrisolti:
Negli anni compresi fra il 1895 ed il 1915 maturano molte delle scoperte e delle idee che hanno portato alla nascita della fisica quantistica e della teoria della relatività:
Fu così che nacque la fisica moderna, nel primo trentennio del XX secolo rappresentata dalla fisica quantistica, che studia il comportamento del mondo atomico e subatomico e dalla fisica della relatività, che si occupa dei sistemi a velocità dell’ordine di grandezza della luce.
La fisica moderna getta le basi per la comprensione della natura a livello atomico, modificando alcuni concetti della fisica classica ed introducendone di nuovi.
In particolare, la sua principale affermazione riguarda il comportamento duale della luce, sia come onda che come particella; simmetricamente, a livello microscopico, ogni particella ha in se un comportamento duale.
Ma non modifica la fisica classica per quanto riguarda il mondo macroscopico.
Ma andiamo per ordine
Spettro del corpo nero.
Un corpo nero non è necessariamente un corpo di colore nero; è un corpo in grado di assorbire tutta la radiazione e.m. che incide su di esso.
Il corpo nero ideale è anche un radiatore (emettitore) ideale, poiché ogni corpo emette le radiazioni che è in grado di assorbire (perciò emette tutte le radiazioni);
inoltre i corpi neri sono “radiatori” universali, perché, ad una data temperatura, presentano tutti lo stesso spettro di emissione in funzione delle frequenze (o delle lunghezze d'onda), indipendentemente dal materiale.
Una stella come il Sole, per esempio, può essere considerata con buona approssimazione un corpo nero. Essa assorbe la radiazione incidente senza rifletterla, ma allo stesso tempo emette luce propria.
Si ottiene un corpo nero utilizzando un blocco di metallo con una cavità accessibile solo tramite un piccolo foro: La radiazione em entra attraverso la fessura e continua ad essere riflessa dalle pareti con poca probabilità di uscire, finché viene completamente assorbita.
I fisici erano interessati a studiare il comportamento del corpo nero al variare della temperatura; per questo motivo il corpo nero è una fornace con le pareti annerite ed un piccolo foro di ingresso.
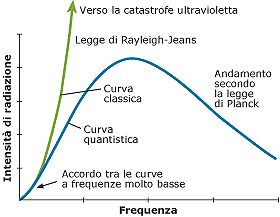
Studio della Radiazione del corpo nero
Semplici esperimenti di irraggiamento da parte del corpo nero hanno evidenziato la curva sperimentale a campana indicata in figura che indica l’Intensità di radiazione, proporzionale al numero di “fotoni” presenti nella cavità, in funzione della frequenza della radiazione em;
curva completamente diversa da quella deducibile dalle leggi della fisica classica e soprannominata “catastrofe ultravioletta”.
f picco = 5,88 1010 T
λpicco = c/fpicco
e la legge di Stefan – Boltzmann:
I = σT4
l'energia irradiata I, per unità di superficie ed unità di tempo è proporzionale alla quarta potenza della temperatura assoluta. La costante di Boltzmann è σ = 5,7 10-8 W(m2K4)
Spettro del corpo nero e Crisi della fisica classica
La fisica classica osservò che il campo em poteva scambiare energia con gli atomi di un corpo.
Ad esempio: un corpo si riscalda perché assorbe radiazione em, oppure la radiazione em assorbita può generare reazioni chimiche.
La fisica classica, inoltre, non poneva nessun limite all’energia elettromagnetica che un corpo può assorbire ed emettere: un corpo può assorbire energia di qualunque frequenza con continuità, raggiungendo valori elevatissimi nell'intervallo dell'UV, ma la catastrofe UV, non si verificava. L’andamento “finito” dello spettro di emissione del corpo nero evidenziava un limite al valore dell’energia scambiata fra corpo nero e radiazione em., limite che cresce con la frequenza, ma che non può essere superato.
I quanti di Planck.
Il fisico tedesco Planck, nel 1899, formulò una teoria rivoluzionaria che gli valse il premio Nobel nel 1918.
Egli ipotizzò che gli scambi di energia fra gli atomi del metallo e la radiazione em avvengano a “pacchetti”, che definisce “quanti di energia” proporzionali alla frequenza dell'onda incidente;
se f è la frequenza della radiazione em incidente, l’energia E che può essere scambiata con il corpo nero è un multiplo intero della la frequenza f :
E = hf
h = 6,6310-34 Js
h è la costante di Planck, considerata ormai una delle costanti fondamentali della natura.
Questa ipotesi comporta che l’energia è quantizzata (come la carica elettrica) e non può assumere tutti i valori; può assumere solo valori discreti e può variare per salti quantizzati molto piccoli, come si vede dal valore di h.
Con queste nuove basi, Planck trova una spiegazione allo spettro del corpo nero ed una formulazione matematica che lo spiega; infatti rifacendo i conti teorici in base alla sua nuova ipotesi, Planck ottiene una curva che riproduce esattamente i dati sperimentali, scongiura la catastrofe uv, introdusse la natura corpuscolare della luce.
Lo stesso Planck non era però soddisfatto e pensava di avere costruito un espediente matematico ad hoc utile per spiegare il fenomeno “corpo nero”.
Ma ogni dubbio cadde grazie ad Einstein e all’effetto fotoelettrico. Einstein fu l’unico a prendere sul serio la teoria dei quanti di Planck e, addirittura l’applicò alla luce, affermando che:
Effetto fotoelettrico.
L'effetto fotoelettrico consiste nell'emissione di elettroni da parte di una superficie metallica (specie alcalina) solo quando viene colpita da radiazione em di frequenza opportuna.
L’effetto fotoelettrico fu osservato, inconsapevolmente, da Hertz, deve il suo nome a Righi, valse il Premio Nobel sia a Lenard (1905) perché lo studiò che ad Einstein (1921) perché lo interpretò. Infine, aprì la discussione sia sull’esistenza o meno dei quanti di luce, introdotti per la prima volta da Plank, per spiegare il comportamento del corpo nero, che alla duplice natura della luce.
Nel 1887 Heirich Hertz dimostra sperimentalmente sia l’esistenza delle onde elettromagnetiche, sia che la loro velocità è uguale a quella della luce (c ≈ 3,0*108 m/s), conferendo, così, validità alla teoria elettromagnetica di Maxwell.
Inoltre nota che alcuni metalli esposti a radiazione em si scaricano, cioè perdono elettroni.
L’anno successivo, Augusto Righi osserva, invece, che sottoponendo a radiazione ultravioletta due elettrodi nasce un arco voltaico, ossia gli elettroni di conduzione del metallo acquistano energia sufficiente per vincere l'attrazione del reticolo ed uscire dal metallo; battezza tale fenomeno effetto fotoelettrico.
Nel 1899, quattro anni dopo la scoperta dell'elettrone ad opera di Thomson, gli scienziati ipotizzano che le particelle emesse dai metalli colpiti dalla radiazione em siano proprio gli elettroni.
Thomson e successivamente Lenard, eseguono esperimenti sul fenomeno fotoelettrico, e scoprono che
Ad esempio la fsoglia di zinco e magnesio è nell’UV, quella del sodio nella zona del visibile.
Questi aspetti dell'effetto fotoelettrico risultavano incomprensibili alla fisica classica e furono spiegati in via teorica da Einstein utilizzando la teoria dei quanti; successivamente Millikan verificò sperimentalmente le ipotesi di Einstein utilizzando una fotocellula (circuito contenuto in un tubo a vuoto formato da un generatore ed un reostato).
L’esperienza ha mostrato le caratteristiche dell’effetto fotoelettrico
Effetto fotoelettrico e Crisi della fisica classica
La soglia fotoelettrica non è spiegabile con la fisica classica: un elettrone fuoriesce se si fornisce un’energia uguale al lavoro di estrazione Lestrazione (= numericamente uguale al potenziale intrinseco, ma espresso in eV), caratteristico di ogni metallo. L’energia è fornita dalla componente elettrica della radiazione em, che accelera l’elettrone aumentandone l’energia cinetica;
la componente elettrica cresce con l’intensità della radiazione em e aumentando l’intensità (non la frequenza) l’elettrone dovrebbe aumentare la propria energia, rompere il legame con il reticolo ed andare in conduzione. Ma ciò non acccade, Al contrario ogni metallo presenta una frequenza di radiazione ben definita per poter emettere elettroni e l'emissione è immediata (avviene alla velocità della luce c).
Einstein spiega l’effetto fotoelettrico
Einstein assume che la radiazione em scambia energia con il metallo in modo discontinuo, cioè discreto, assorbendo singoli fotoni (1, 2,... mai 1/, 2/3..di fotone).
Il fotone di energia E =hf incide sul metallo, interagisce con un singolo elettrone e viene assorbito. Il fotone scompare e l’energia dell’elettrone aumenta della quantità E=hf.
L'elettrone, però, sfugge al reticolo metallico solo se acquista un'energia uguale o superiore al lavoro di estrazione Lestrazione.
Si ha quindi la condizione Lestrazione = h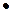 fsoglia da cui si ottiene
fsoglia da cui si ottiene
fsoglia =
se fincidente < f soglia l'energia che il fotone comunica all'elettrone nell'urto è minore del lavoro di estrazione e non produce foto-emissione ma un aumento della temperatura del reticolo.
Se fincidente = > f soglia, l'elettrone assorbe dal fotone energia uguale o maggiore a quella di estrazione e fuoriesce dal metallo.
L'eventuale surplus di energia rappresenta l'energia cinetica con cui l'elettrone si allontana.
Ecin = h∙ fincidente – Lestrazione.
Per la spiegazione dell'effetto fotoelettrico Einstein ottenne il premio Nobel nel 1921.
Ricordando la relazione c=λ∙f, è facile dedurre la lunghezza d’onda di soglia per l’effetto fotoelettrico.
L’effetto fotoelettrico e la natura della luce.
L'interpretazione dell'effetto fotoelettrico con la conseguente accettazione della teoria dei quanti di Planck mette in luce la natura corpuscolare e non ondulatoria (Maxwell) della luce: i fotoni di luce sono visti come “proiettili” che colpiscono l'elettrone cedendo energia (urto elastico) ed in moto con quantità di moto
p = 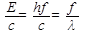
Da qui si fa strada l’idea della doppia natura della luce. Questa ipotesi non deve stupire.
Infatti anche l’uomo si comporta da figlio, marito, padre, uomo d’affari a seconda delle circostanze e dell’ambiente: non si comporta da marito con un cliente, eppure nessuno si stupisce di ciò.
Quindi la luce manifesta proprietà corpuscolari o ondulatorie a seconda della situazione in cui si trova.
Born dirà che gli esperimenti volti a provare la natura ondulatoria della luce non possono in nessun modo mettere in evidenza la sua natura corpuscolare e viceversa, sostenendo questa affermazione nel principio di complementarietà.
Applicazione dell'effetto fotoelettrico.
La tecnologia di uso quotidiano utilizza largamente l’effetto fotoelettrico, di cui siamo “inconsapevoli” spettatori ogni volta che prendiamo l’ascensore ed osserviamo il funzionamento a scorrimento delle sue porte. Un raggio luminoso, infatti, attraversa lo specchio della porta aperta; lo stesso raggio luminoso colpisce una cellula fotoelettrica per produrre elettroni che attivano il circuito elettrico di chiusura della porta. Il raggio luminoso viene interrotto dal nostro passaggio; in questo modo si interrompe la corrente elettrica, così da impedire che la porta si richiuda.
Gli impieghi sono molteplici e vanno dai dispositivi d'allarme agli automatismi per cancelli o porte, inoltre i cronometri di molte discipline sportive sono collegati a fotocellule. Le cellule fotoelettriche possono comandare l'accensione di lampade a seconda della luminosità presente, negli anni 60 alcuni costruttori di televisori impiegavano una fotocellula per adeguare la luminosità dell'immagine in bianco e nero, alla luminosità dell'ambiente.
I fotoni e le nuove formule fisiche.
Il termine fotone è stato usato per la prima volta nel 1926 da Lewis ed identifica una particella di luce; tuttavia differisce dalle comuni particelle.
Le particelle classiche si possono toccare e pesare perchè dotate di massa.
Il fotone si muove alla velocità della luce
![]()
uguale per tutti gli osservatori e non può essere toccato, non può essere raggiunto e non può essere pesato poiché ha massa a riposo nulla. non decade spontaneamente ed ha vita media infinita.
La sua massa a riposo è nulla, ma ha energia a riposo E0 = mc2
La sua energia E, è:
![]()
oppure
E=hf
![]()
![]()
dove k è il vettore d'onda di modulo k = 2π/λ, ω = 2πν la frequenza angolare e ħ = h/2π la costante di Planck ridotta.
Nonostante la massa a riposo sia nulla, è possibile definire una massa equivalente a partire dalla relazione di Einstein E=mc² che risulta essere pari a
![]()
L'effetto Compton.
L'effetto Comptom porta alla completa accettazione della teoria della quantizzazione dell'energia e conferma la natura corpuscolare della luce.
Dopo l'interruzione causata dalla prima guerra mondiale, nel 1923, Arthur Compton conferma sperimentalmente la natura corpuscolare della radiazione em, studiando la diffusione dei raggi X da parte di un campione di grafite: i raggi X deviati dagli elettroni della grafite variano la lunghezza d'onda (frequenza), assumendo
λfinale > λincidente.
f finale < f incidente
il fotone diffuso ha un’energia inferiore di quello incidente
Effetto Compton e Crisi della fisica classica
Come per l'effetto fotoelettrico e per il corpo nero, questo risultato è incomprensibile sulla base delle leggi della teoria ondulatoria classica della luce, secondo la quale i raggi X incidenti dovrebbero essere diffusi in tutte le direzioni, con la medesima lunghezza d'onda, contrariamente ai risultati sperimentali.
Secondo la fisica classica la radiazione X colpisce un elettrone fermo e libero da legami mettendolo in oscillazione alla sua stessa frequenza; l’elettrone, a sua volta, irradia una radiazione em della stessa frequenza incidente, comportandosi come un circuito oscillante/antenna.
Compton dimostra la natura corpuscolare della luce.
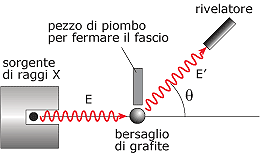
Considerando la radiazione come un corpuscolo, dotato di energia e di quantità di moto, Compton studia l'interazione tra fotone (radiazione X) – elettrone (del reticolo di grafite) come un urto elastico ed applica le leggi di conservazione dell'energia e della quantità di moto in forma relativistica (a causa delle velocità coinvolte); ottiene, così, una relazione che esprime la variazione di lunghezza d'onda dei raggi X in funzione dell'angolo di deviazione del fascio incidente.
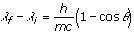
dove h è la costante di Planck,
m è la massa dell'elettrone
c è la velocità della luce.
Con λ Compton. = h/mc =
Storicamente l'effetto Compton è importante perché convinse in maniera pressoché definitiva la comunità scientifica che la radiazione elettromagnetica possiede una natura corpuscolare

Formule:
hf1= hf2 + E cin,elettrone
hf1/c = hf2 /c cosθ + p elettrone cosφ
oppure
h/λ1= h/λ2 cosθ + p elettrone cosφ
0 = hf2/c sinθ + p elettrone sinφ
0 = hc/λ2 sinθ + p elettrone sinφ
si ottiene la variazione della lunghezza d'onda del fotone per effetto della diffusione:
Crisi del modello atomico classico.
Secondo il modello “planetario” di Rutheford, gli elettroni dovrebbero cadere sul nucleo in circa un centesimo di microsecondo ed emettere radiazioni con spettro continuo, in contraddizione con i dati sperimentali, cioè
Per superare le contraddizioni legate al modello di Rutheford, Niel Bohr utilizza la teoria quantistica avanzando le seguenti ipotesi:
in base a queste ipotesi, Bohr assume che gli atomi hanno livelli energetici discreti di cui occupano il più basso, detto livello fondamentale. Per salire ai livelli superiori, detti eccitati, deve assorbire energia dal fotone di frequenza
f = 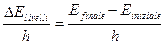
Altri esponenti della fisica quantistica.
Louis De Broglie e l'unificazione onda – corpuscolo.
La teoria dei quanti di energia di Planck consolidava la duplice natura (onda-corpuscolo) della radiazione em e rivela il comportamento ondulatorio o corpuscolare a seconda dell'esperimento e dl fenomeno studiato.
Nel 1924 il francese Louis De Broglie suggerisce di estendere a tutti i corpi, anche materiali, la duplice natura (corpuscolare e ondulatoria) già osservata per la radiazione elettromagnetica e di associare a ogni particella un'onda, detta onda di materia, di lunghezza d'onda
λ = 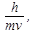
dove m è la massa della particella e v la sua velocità, h la costante di Planck
L'ipotesi di De Broglie venne confermata nel 1927 dai risultati di una serie di esperimenti di interazione elettrone-cristallo condotti dai fisici statunitensi Clinton Joseph Davisson e Lester Halbert Germer, oltre che dal fisico britannico George Paget Thomson.
Wolfgang Pauli e la comprensione della tavola periodica
Nel 1925 il fisico austriaco Wolfgang Pauli enuncia il principio di esclusione che stabilisce un limite per il numero di elettroni che possono occupare un determinato livello energetico; trovano così giustificazione le diverse proprietà dei singoli elementi chimici e si inizia a comprendere la struttura della tavola periodica.
Werner Heisenberg ed un limite alle misure microscopiche.
Nel 1927 Heisenberg formula il principio di indeterminazione, con il quale viene riconosciuta l'esistenza di un limite naturale alla precisione con cui si possono misurare simultaneamente alcune coppie di grandezze fisiche, quali ad esempio posizione e quantità di moto ed energia e tempo.
Avvalorando l'ipotesi di De Broglie, se una particella non è un oggetto puntiforme, come
facciamo a dire dove si trova e con quale velocità si muove, dato che un’onda non sta in un posto preciso ?
Secondo il principio di indeterminazione di Heisenberg è impossibile determinare contemporaneamente sia la posizione sia la quantità di moto di un corpo.
Analogamente è impossibile determinare contemporaneamente sia la velocità sia l’energia di un corpo.
Ma tra queste coppie di grandezze esiste una disuguaglianza:
Δx Δp > h
ΔE Δt > h
Nel 1928 Dirac giunse a una sintesi della meccanica quantistica e della relatività, grazie alla quale si previde l'esistenza del positrone e più in generale dell’antimateria.
Erwin Schrodinger e l'onda di probabilità.
Nel 1925 Schrodinger elabora una teoria in grado di spiegare il comportamento degli atomi con molti elettroni.
Si tratta di un'equazione basata sulla teoria onda – corpuscolo della materia di De Broglie e la cui soluzione è detta funzione d'onda.
La funzione d'onda esprime la probabilità di trovare un elettrone in una data posizione dello spazio atomico; all'elettrone è associata un'onda che corrisponde ad una nuvola di probabilità che circonda il nucleo.
Questa nuvola fu chiamata orbitale; entro gli orbitali c'è una probabilità del 90% di trovare l'elettrone.
La probabilità del gatto di Schrodinger
In una stanza perfettamente isolata dall'esterno, un perfido fisico chiude
L'atomo è in uno stato tale per cui, a una certa ora, avrà uguale probabilità di essere o no decaduto. Il fisico ha anche collegato l'atomo al veleno in modo che questo sia liberato se l'atomo decade. Il veleno è abbastanza potente da uccidere immediatamente il gatto.
All'ora convenuta il fisico aprirà la stanza. Cosa troverà? Un attimo prima dell'apertura, lo stato che descrive il sistema totale della stanza (atomo più fiala più gatto) sarà
La funzione d’onda di Scrodinger descrive l’onda di materia conoscendo tempo e spazio; essa indica la probabilità di trovare la particella in una data posizione ed in un dato istante per unità di volume. Una particella ha una certa probabilità di trovarsi in una zona in cui non potrebbe mai trovarsi per la fisica classica.
Spettro elettromagnetico |
frequenza |
Lunghezza |
Onde radio |
< 3 Ghz |
> 10 cm |
Microonde |
3 GHz – 300 GHz |
1mm – 10cm |
Infrarossi |
300 GHz – 428 THz |
700nm – 1 mm |
Luce visibile |
428 THz – 749 THz |
400 nm – 700 nm |
Ultravioletti |
749 THz – 30 PHz |
10 nm – 400 nm |
Raggi X |
30 PHz – 300 EHz |
1 pm – 10 nm |
Raggi gamma |
> 300 EHz |
< 1 pm |
Fonte: http://sorsidifisica.weebly.com/uploads/3/4/6/0/3460712/fisica_quantistica_2012_4_al.doc
Sito web da visitare: http://sorsidifisica.weebly.com/
Autore del testo: non indicato nel documento di origine
Il testo è di proprietà dei rispettivi autori che ringraziamo per l'opportunità che ci danno di far conoscere gratuitamente i loro testi per finalità illustrative e didattiche. Se siete gli autori del testo e siete interessati a richiedere la rimozione del testo o l'inserimento di altre informazioni inviateci un e-mail dopo le opportune verifiche soddisferemo la vostra richiesta nel più breve tempo possibile.
I riassunti , gli appunti i testi contenuti nel nostro sito sono messi a disposizione gratuitamente con finalità illustrative didattiche, scientifiche, a carattere sociale, civile e culturale a tutti i possibili interessati secondo il concetto del fair use e con l' obiettivo del rispetto della direttiva europea 2001/29/CE e dell' art. 70 della legge 633/1941 sul diritto d'autore
Le informazioni di medicina e salute contenute nel sito sono di natura generale ed a scopo puramente divulgativo e per questo motivo non possono sostituire in alcun caso il consiglio di un medico (ovvero un soggetto abilitato legalmente alla professione).
"Ciò che sappiamo è una goccia, ciò che ignoriamo un oceano!" Isaac Newton. Essendo impossibile tenere a mente l'enorme quantità di informazioni, l'importante è sapere dove ritrovare l'informazione quando questa serve. U. Eco
www.riassuntini.com dove ritrovare l'informazione quando questa serve